
VENTANA MMR RxDx Panel
Interpretationshilfe für
Endometriumkarzinom (EC)
VENTANA anti-MLH1 (M1) Mouse Monoclonal Primary Antibody
VENTANA anti-PMS2 (A16-4) Mouse Monoclonal Primary Antibody
VENTANA anti-MSH2 (G219-1129) Mouse Monoclonal Primary Antibody
VENTANA anti-MSH6 (SP93) Rabbit Monoclonal Primary Antibody


Inhaltsverzeichnis
Einleitung 1
Verwendungszweck 3
Verwendungszweck des Produkts 3
Zweck der Interpretationshilfe 3
Klinische Auswertung 4
Färbungseigenschaften 4
Akzeptanzkriterien für Morphologie und Hintergrund 5
Fallkriterien für die klinische Auswertung 5
Bewertungsalgorithmus 6
Kontrollen 8
Interne positive Kontrollen 8
Proben-Workflow 10
Referenzbilder 12
Fälle mit positivem Expressionssignal 12
Fälle mit defizienter Expression 14
Schwierige Fälle 18
Einfluss präanalytischer Bedingungen auf das VENTANA MMR RxDx Panel 28
Geeignete Fixierungsbedingungen zur Erzielung optimaler Färbeergebnisse 28
Stabilität des Gewebeschnitt-Objektträgers 32
Gewebedicke 32
Literaturangaben 33


Die DNA-Mismatch-Reparatur (MMR) ist ein konservierter
molekularer Mechanismus, der dazu dient, bei der DNA-
Replikation spontan auftretende falsche Basensubstitutionen
zu korrigieren. Methoden auf Basis der Polymerase-
Kettenreaktion (PCR) ergaben, dass ein Versagen der MMR
häufig zu Mikrosatelliteninstabilität (MSI) führt, bei der kurze,
aufeinanderfolgende Nukleotid-Wiederholungen in die DNA
eingefügt werden. Wenn die Anzahl der Wiederholungen gleich
oder größer als 30% der untersuchten Mikrosatelliten-Loci ist,
wird dies als MSI-High (MSI-H) bezeichnet. Defekte in der MMR-
Maschinerie wurden auf Mutationen in den MMR-Proteinen
zurückgeführt, am häufigsten in MLH1, PMS2, MSH2 und MSH6.
Die Proteine MLH1 und PMS2 bilden ebenso wie die Proteine
MSH2 und MSH6 normalerweise einen heterodimeren Komplex.
Wenn die MMR normal funktioniert, bindet das MSH6/MSH2-
Heterodimer an die Mismatch-DNA. Diese Bindung induziert eine
Konformationsänderung, die es dem MLH1/PMS2-Heterodimer
ermöglicht, den DNA-gebundenen MSH6/MSH2-Komplex zu
binden, was zu einer Exzisionsreparatur der betroffenen DNA
führt. Mutationen in oder Mängel an diesen Proteinen führen zu
einer erhöhten Häufigkeit von MSI und somatischen Mutationen
durch Replikationsfehler. Zur Identifizierung von MMR-Genen
mit erhöhter Wahrscheinlichkeit für Keimbahn- oder somatische
Veränderungen haben sich immunhistochemische (IHC) MMR-
Tests als hilfreich erwiesen.
Bislang richtet sich der Behandlungsplan für Krebspatienten
nach der jeweils vorliegenden malignen Erkrankung. Neue
Immuntherapien, insbesondere solche, die zelluläre Signalwege
modifizieren, an denen die Proteine PD-1 (Programmed
Death-1) oder PD-L1 (Programmed Death Ligand 1) beteiligt
sind, ermöglichen jedoch eine gezieltere Anpassung der
therapeutischen Strategien. PD-1 ist ein inhibierender Rezeptor,
der auf aktivierten T-Zellen exprimiert wird. Dieser Zustand
wird bei chronischer Stimulation wie etwa bei chronischen
Infektionen oder bei Krebs beibehalten. PD-L1-Expression
wurde bei Immunzellen und malignen Zellen festgestellt, und
es wurde berichtet, dass eine anomale Expression von PD-L1
auf Tumorzellen (TC) die Anti-Tumor-Immunität behindert, was
eine Immunevasion zur Folge hat. Aus diesem Grund stellt die
Unterbrechung des PD-L1/PD-1-Wegs eine aussichtsreiche
Strategie zur Stärkung der tumorspezifischen Immunität der
T-Zellen dar.
MMR-Proteine (MLH1, PMS2, MSH2 und MSH6) werden in
proliferierenden normalen und malignen Zellen ubiquitär
exprimiert. Bei vielen häufigen Formen von Krebs liegen eine
MMR-Defizienz (dMMR) und eine MSI vor. In mehreren Studien
wurde gezeigt, dass eine MMR-Defizienz mit einer höheren
Expression von PD-1- oder PD-L1-Proteinen korreliert.
Somit sind MMR-Proteine möglicherweise nützliche prädiktive
Biomarker für eine auf PD-1 abzielende Therapie. Insbesondere
könnte ein Verlust der Expression eines oder mehrerer MMR-
Proteine auf eine erhöhte Wahrscheinlichkeit des Ansprechens auf
eine solche Therapie hindeuten. PD-1-Inhibitoren können bei
vielen häufigen Krebserkrankungen mit hoher Häufigkeit einer
MMR-Defizienz und/oder MSI-H unabhängig vom jeweiligen
Ursprungsgewebe von Vorteil sein. Daher ist es sinnvoll, bei
Patienten, für die eine auf PD-1 abzielende Therapie in Betracht
kommt, einen begleitenden diagnostischen Assay durchzuführen,
um die Patientenpopulation mit MMR-Defizienz zu identifizieren.
Endometriumkarzinome (EC) zählen zu den häufigsten
gynäkologischen Krebserkrankungen.
12
Häufig liegen bei diesen
Tumoren zahlreiche genetische Veränderungen einschließlich
MSI vor.
12
Darüber hinaus wurde bereits vermutet, dass EC
mit MSI im Vergleich zu mikrosatellitenstabilen (MSS) EC eine
erhöhte PD-L1-Proteinexpression aufweisen.
16
Zwar variiert
die Behandlung von EC je nach Grad, Histologie und Stadium
der Erkrankung,
17
aber die Feststellung des MMR-Status
von EC-Tumoren ist für die Erstellung einer Prognose und als
Behandlungsgrundlage stets von Nutzen
12
. Daher ist es sinnvoll,
bei Patienten, für die eine auf PD-1 abzielende Therapie in
Betracht kommt, einen begleitenden diagnostischen Assay zur
Feststellung des MMR-Status durchzuführen.
Ein Verlust der Expression eines der essentiellen MMR-Proteine,
zu denen MLH1, PMS2, MSH2 und MSH6 zählen, verursacht
eine MMR-Defizienz. Das Vorhandensein einer Färbung für
alle vier MMR-Proteinmarker im Tumor bedeutet, dass der
Fall einen positiven VENTANA MMR IHC-Status aufweist. Eine
fehlende Färbung für nur einen der MMR-Proteinmarker mit dem
VENTANA MMR RxDx Panel bedeutet einen negativen VENTANA
MMR IHC-Status.
Einleitung
VENTANA MMR RxDx Panel für Endometriumkarzinom 1

2 VENTANA MMR RxDx Panel für Endometriumkarzinom

Verwendungszweck
Verwendungszweck des Produkts
Eine ausführliche Beschreibung des Verwendungszwecks dieses
Produkts einschließlich der dazugehörigen Indikationen ist in
der Packungsbeilage des jeweiligen VENTANA MMR RxDx Panel
enthalten.
Zweck der Interpretationshilfe
Diese Anleitung dient:
• Als Hilfe für Pathologen bei der klinischen Auswertung von
Schnitten von formalinfixiertem, paraffineingebettetem
(FFPE) Tumorgewebe, die entsprechend der jeweiligen
Produktbeschreibungen mit dem VENTANA MMR RxDx Panel
gefärbt worden sind.
• Zur Bereitstellung von Fotoaufnahmen, die die Färbemuster
illustrieren, die sich aus der Färbung von Tumorgeweben mit
dem VENTANA MMR RxDx Panel ergeben können.
• Zur Bereitstellung von Beispielbildern schwieriger Fälle, die zu
deren Beurteilung herangezogen werden können.
• Zur Bereitstellung einer Anleitung zur Verwendung von MMR-
Protein-positiven normalen Gewebebestandteilen, die bei
einer Färbung mit dem VENTANA MMR RxDx Panel als interne
positive Kontrolle dienen.
VENTANA MMR RxDx Panel für Endometriumkarzinom 3

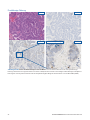
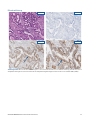
Färbestatus „Intakte Expression von MMR“ und „Verlust der Expression von MMR“: Bei diesen Fällen von
Endometriumkarzinomen weisen die Zellkerne eindeutig das vorherrschende Färbemuster auf, das bei den meisten Tumorgeweben mit
intakter Expression von MSH6 vorliegt (linkes Panel). Nichtvorhandensein einer Zellkernfärbung in Tumorgewebe bedeutet einen
Verlust der Expression von MSH6 (rechtes Panel). Eine eindeutige Zellkernfärbung in internen Kontrollzellen (d.h. Lymphozyten) in
der Nähe lebensfähiger Tumoren dient als akzeptable interne positive Kontrolle.
Färbungseigenschaften
Klinische Auswertung
Mit jedem der Assays im VENTANA MMR RxDx Panel markierte
Zellen werden auf das Vorhandensein oder Fehlen des
Diaminobenzidin(DAB)-Signals untersucht. Die Färbung von
MMR-Proteinen mit dem VENTANA MMR RxDx Panel folgt einem
nukleären Muster. Der Verlust der Expression eines der mit dem
VENTANA MMR RxDx Panel nachgewiesenen MMR-Proteine
ist im Zellkern von Tumorzellen festzustellen. Der MMR-Status
wird ausschließlich auf der Grundlage einer eindeutigen
Zellkernfärbung als „Intakt“ oder „Verlust“ eingestuft.
• Bei einem Status „Intakt“ sind Tumorzellen mit eindeutiger
Färbung vorhanden, die gleich der oder stärker als die
Intensität in den internen Kontrollen über dem Hintergrund ist.
• Bei einem Status „Verlust“ ist kein nachweisbares Signal
vorhanden. Bei Fällen mit Status „Verlust“ kann trotzdem eine
hellgraue Verfärbung der Zellkerne vorliegen.
Das Signal kann homogen verteilt sein und eine gleichmäßige
Intensität in den neoplastischen Abschnitten des Tumors
aufweisen oder heterogen verteilt sein und unterschiedliche
Intensitätsstufen aufweisen. Es sollte bei schwacher Vergrößerung
wie beispielsweise 2x oder 4x leicht erkennbar sein. Der Abschnitt
Referenzbilder in dieser Interpretationshilfe enthält Bildmaterial
von neoplastischen Zelltypen/Färbungselementen nach Färbung
mit dem VENTANA MMR RxDx Panel. Zur Bewertung des
vorhandenen Hintergrunds in Testproben und zur Festlegung
einer Baseline für die Färbeintensität wird die speziesspezifische
negative Reagenzkontrolle (NRC) verwendet. In Tabelle1 sind
Akzeptanzkriterien für Morphologie und Hintergrund aufgeführt.
In Tabelle2 sind fallspezifische Kriterien zur Bewertung des MMR-
Status von neoplastischem Gewebe mit einem der vier Assays im
VENTANA MMR RxDx Panel angegeben.
Tumorzellen ohne
Zellkernfärbung
Eindeutige Zellkernfärbung
in Tumorzellen
Starke Zellkernfärbung
in Lymphozyten
4 VENTANA MMR RxDx Panel für Endometriumkarzinom
MSH6 10x MSH6 10x

Akzeptanzkriterien für Morphologie und Hintergrund
Für jeden mit dem VENTANA MMR RxDx Panel gefärbten Fall wird die Akzeptanz der Gewebemorphologie und des Hintergrundes
anhand der in Tabelle1 beschriebenen Kriterien geprüft.
Fallkriterien für die klinische Auswertung
In Tabelle2 sind die Kriterien für die Auswertung eines Objektträgers mit neoplastischem Gewebe hinsichtlich des MMR-Status mit
einem der Assays im VENTANA MMR RxDx Panel zusammengefasst.
Kriterium Akzeptabel Nicht akzeptabel
Morphologie Es sind zelluläre Elemente von Interesse zu
sehen, was eine klinische Interpretation einer
spezifischen Färbung ermöglicht
Es sind keine zellulären Elemente von Interesse
zu sehen, was eine klinische Interpretation einer
spezifischen Färbung erschwert
Hintergrund Der Hintergrund hat keinen störenden
Einfluss auf die klinische Interpretation einer
spezifischen Färbung
Der Hintergrund hat einen störenden Einfluss auf
die Möglichkeit der Interpretation einer spezifischen
Färbung
Tabelle1: Akzeptanzkriterien für Morphologie und Hintergrund
Klinische Interpretation Färbemuster-Kriterien
Auswertbar (alle Kriterien müssen
zutreffen)
1. H&E ergibt ≥50lebensfähige Tumorzellen
2. Objektträger mit der Negative Reagent Control ist akzeptabel
3. Morphologie ist akzeptabel
4. Hintergrund ist akzeptabel
5. Interne positive Kontrollen weisen eine eindeutige Zellkernfärbung auf
Nicht auswertbar (wenn ein Kriterium in
diesem Abschnitt zutrifft, sollte ggf. die
Objektträgerfärbung wiederholt oder das
Ergebnis nicht berücksichtigt werden)
1. H&E ergibt <50lebensfähige Tumorzellen
2. Objektträger mit der Negative Reagent Control ist nicht akzeptabel
3. Morphologie ist nicht akzeptabel
4. Hintergrund ist nicht akzeptabel
5. Interne positive Kontrollen weisen keine eindeutige Zellkernfärbung auf
6. Interpretation ist aufgrund von Gewebeverlust, Nichtvorhandensein von
Tumorgewebe, Artefakten und/oder Randartefakten nicht möglich
Tabelle2: Kriterien für die Auswertbarkeit
VENTANA MMR RxDx Panel für Endometriumkarzinom 5

Das VENTANA MMR RxDx Panel umfasst vier Assays: VENTANA
anti-MLH1 (M1) Mouse Monoclonal Primary Antibody, VENTANA
anti-PMS2 (A16-4) Mouse Monoclonal Primary Antibody,
VENTANA anti-MSH2 (G219-1129) Mouse Monoclonal Primary
Antibody und VENTANA anti-MSH6 (SP93) Rabbit Monoclonal
Primary Antibody. Für die Färbung mit jedem dieser Antikörper
wird ein serieller Gewebeschnitt der Testprobe benötigt. Für
die Färbung mit Hämatoxylin und Eosin (H&E) und mit NRC-
Antikörpern, die der Spezies des jeweiligen VENTANA MMR RxDx
Panel-Antikörpers (Negative Control (Monoclonal) (mNRC) oder
Rabbit Monoclonal Negative Control Ig (rNRC)) entsprechen,
werden weitere serielle Gewebeschnitte der Testprobe benötigt.
Mit dem VENTANA MMR RxDx Panel gefärbte neoplastische
Zellen werden hinsichtlich des Vorhandenseins oder
Fehlens des DAB-Signals beurteilt. Der passende mit NRC
gefärbte Objektträger wird verwendet, um die unspezifische
Hintergrundfärbung sowie den Grad der bekanntermaßen
aufgrund bestimmter Gewebebestandteile auftretenden
Hintergrundfärbung zu bewerten (bitte das Bildmaterial zu Fällen
mit positivem und negativem Signal beachten).
Wenn die Auswertung der H&E-Färbung ergibt, dass die
Patientenprobe ungeeignet ist (z.B. wenn weniger als
50lebensfähige Tumorzellen vorhanden sind), sollte eine neue
Probe entnommen werden.
Die wiederholte Färbung einer Probe mit einem bestimmten
MMR RxDxAssay aus dem Panel (z.B. VENTANA anti-MLH1
(M1) Mouse Monoclonal Primary Antibody) sollte auf nicht
gefärbten Objektträgern durchgeführt werden, wenn (1) der
mit der entsprechenden NRC für den jeweiligen Assay gefärbte
Fall-Objektträger keine akzeptable Färbung aufweist oder (2) der
mit dem jeweiligen MMR RxDx Assay (z.B. VENTANA anti-MLH1
(M1) Mouse Monoclonal Primary Antibody) gefärbte Objektträger
nicht auswertbar ist. Wenn einer der Objektträger aufgrund einer
fehlenden Färbung in den als interne positive Kontrolle dienenden
Zellen, des Vorhandenseins von Artefakten, Randeffekten,
Nekrose, eines Gewebemangels oder aus anderen Gründen nicht
interpretierbar ist, ist eine Auswertung dieses Objektträgers nicht
möglich. Wenn die Kontrollfärbung akzeptabel ist und die mit dem
VENTANA MMR RxDx Panel gefärbten Objektträger auswertbar sind,
kann das Färbeergebnis von einem geschulten Pathologen unter
Heranziehung des Bewertungsalgorithmus ausgewertet werden.
HINWEIS: Als Nachweisreagenzien für die Verwendung mit dem
VENTANA MMR RxDx Panel werden nur OptiView DAB IHC
Detection Kit und OptiView Amplification Kit empfohlen.
In den Tabellen 3 und 4 ist die Interpretation der Proteinexpression
bzw. des MMR-Status für das VENTANA MMR RxDx Panel
angegeben. Repräsentative Fälle werden im Abschnitt
Referenzbilder erläutert.
Auswertung des VENTANA MMR RxDx Panel:
Bewertungsalgorithmus
Tabelle4: Interpretation des MMR-Status nach Färbung mit dem VENTANA MMR RxDx Panel
Positiv Negativ
Die Expression aller vier Proteine (MLH1, PMS2, MSH2
und MSH6) in dem Panel ist intakt
Für mindestens eines der Proteine (MLH1, PMS2, MSH2 oder
MSH6) in dem Panel liegt ein Verlust der Expression vor
Tabelle3: Interpretation der Proteinexpression nach Färbung mit dem VENTANA MMR RxDx Panel
Intakte Proteinexpression Verlust der Proteinexpression
Eindeutige Zellkernfärbung in lebensfähigen
Tumorzellen und Vorhandensein akzeptabler
interner positiver Kontrollen (z.B. Zellkernfärbung in
Lymphozyten, Fibroblasten oder normalem Epithel in
der Nähe des Tumors)
Eindeutiger Verlust der Zellkernfärbung oder fokale schwache
nicht eindeutige Zellkernfärbung in den lebensfähigen
Tumorzellen bei Vorhandensein akzeptabler interner positiver
Kontrollen. Eine punktförmige Zellkernfärbung wird als negativ
erachtet.
6 VENTANA MMR RxDx Panel für Endometriumkarzinom

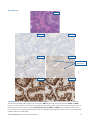
Endometriumkarzinom – Klinische Diagnose mit intakter Expression
Status „Intakte Expression von
MSH2“: Starke Zellkernfärbung bei
Vorhandensein akzeptabler interner
positiver Kontrollen
Status „Intakte Expression von PMS2“:
Starke Zellkernfärbung bei Vorhandensein
akzeptabler interner positiver Kontrollen
Status „Intakte Expression von MLH1“:
Starke Zellkernfärbung bei Vorhandensein
akzeptabler interner positiver Kontrollen
Endometriumkarzinom – Klinische Diagnose mit Expressionsverlust
Status „Verlust der Expression von
MLH1“: Keine Zellkernfärbung bei
Vorhandensein akzeptabler interner
positiver Kontrollen
Status „Verlust der Expression von
MSH6“: Keine Zellkernfärbung bei
Vorhandensein akzeptabler interner
positiver Kontrollen
Status „Verlust der Expression von
MSH2“: Keine Zellkernfärbung bei
Vorhandensein akzeptabler interner
positiver Kontrollen
MLH1 20x MSH6 20x MSH2 20x
MSH2 20x
PMS2 20x
MLH1 20x
MSH2-
positive
Zellkerne
PMS2-
positive
Zellkerne
MLH1-
positive
Zellkerne
VENTANA MMR RxDx Panel für Endometriumkarzinom 7

Kontrollen
Bei Färbung mit dem VENTANA MMR RxDx Panel weisen normale
Gewebebestandteile wie Lymphozyten, Fibroblasten oder normales
Epithel in der Nähe des Tumors eine Färbung der MMR-Proteine im
Zellkern auf. Diese Gewebebestandteile dienen als interne positive
Kontrollen und müssen bei jedem Assay im Panel akzeptabel
sein, um den gefärbten Objektträger auswerten zu können. Die
Auswertung interner Kontrollen ist bei jedem Assay erforderlich.
Dabei müssen die Färbekriterien für eine Panel-Interpretation des
MMR-Status erfüllt sein. Wenn keine eindeutige Zellkernfärbung
in Lymphozyten, Fibroblasten oder normalem Epithel in der Nähe
des Tumors vorliegt, ist der mit dem Assay gefärbte Objektträger als
„nicht auswertbar“ zu betrachten.
In Tabelle5 sind die Kriterien für eine akzeptable Färbung der
internen Kontrolle angegeben.
Auswertbar Nicht auswertbar
Eindeutige Zellkernfärbung in normalen
Gewebebestandteilen (z.B. Lymphozyten, Fibroblasten oder
normales Epithel) in der Nähe des Tumors
Keine eindeutige Zellkernfärbung in normalen
Gewebebestandteilen (z.B. Lymphozyten, Fibroblasten oder
normales Epithel) in der Nähe des Tumors
Tabelle5: Kriterien für die Färbung der internen Kontrolle
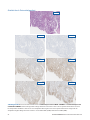
Interne positive Kontrolle, Fall1: Das Endometriumkarzinom weist keine Färbung der internen Kontrolle in der Nähe der Tumorzellen
auf, daher ist keine Auswertung des Karzinoms möglich. Bei der dargestellten akzeptablen Negative Reagent Control handelt es sich um
Maus-NRC (mNRC).
Interne positive Kontrollen
Nachstehend sind repräsentative Abbildungen der internen Kontrolle für das VENTANA MMR RxDx Panel gezeigt.
8 VENTANA MMR RxDx Panel für Endometriumkarzinom
H&E 40x mNRC 40x MLH1 40x

Interne positive Kontrolle, Fall2: Es liegt eine starke Färbung interner Kontrollzellen in Tumornähe eines Falles eines
Endometriumkarzinoms mit Status Verlust der Expression von MLH1 und eines Falles mit Status intakte Expression von MSH2 vor.
Bei der akzeptablen Negative Reagent Control handelt es sich um Maus-NRC (mNRC).
MLH1 20x
Färbung interner Kontrollzellen Färbung interner Kontrollzellen
VENTANA MMR RxDx Panel für Endometriumkarzinom 9
H&E 20x mNRC 20x
MSH2 20x

Proben-Workflow
Für den Test mit dem VENTANA MMR RxDx Panel sind mehrere
serielle Gewebeschnitte je Testprobe erforderlich. Es wird jeweils
ein Gewebeschnitt für die Färbung mit jedem der 4Assays
VENTANA anti-MLH1 (M1) Mouse Monoclonal Primary Antibody,
VENTANA anti-PMS2 (A16-4) Mouse Monoclonal Primary
Antibody, VENTANA anti-MSH2 (G219-1129) Mouse Monoclonal
Primary Antibody und VENTANA anti-MSH6 (SP93) Rabbit
Monoclonal Primary Antibody benötigt. Darüber hinaus werden
von jeder Testprobe Schnitte für die H&E-Färbung und für die
Färbung mit dem NRC-Antikörper entsprechend der Spezies des
jeweiligen VENTANA MMR RxDx Panel-Antikörpers (mNRC oder
rNRC) benötigt.
Wenn die Auswertung der H&E-Färbung ergibt, dass die
Patientenprobe ungeeignet ist (z.B. wenn weniger als
50lebensfähige Tumorzellen vorhanden sind), sollte eine neue
Probe entnommen werden. Die wiederholte Färbung einer Probe
mit einem bestimmten MMR RxDxAssay aus dem Panel (z.B.
VENTANA anti-MLH1 (M1) Mouse Monoclonal Primary Antibody)
sollte auf nicht gefärbten Objektträgern durchgeführt werden,
wenn (1) der mit der entsprechenden negativen Reagenzkontrolle
für den jeweiligen Test gefärbte Fall-Objektträger keine
akzeptable Färbung aufweist oder (2) der mit dem jeweiligen
MMR RxDx Assay (z.B. VENTANA anti-MLH1 (M1) Mouse
Monoclonal Primary Antibody) gefärbte Objektträger nicht
auswertbar ist. Wenn einer der Objektträger aufgrund fehlender
Färbung in den als interne positive Kontrolle dienenden Zellen,
des Vorhandenseins von Artefakten, Randeffekten, Nekrose, eines
Gewebemangels oder aus anderen Gründen nicht interpretierbar
ist, ist eine Auswertung dieses Objektträgers nicht möglich.
Wenn die Kontrollen akzeptabel und die mit dem VENTANA
MMR RxDx Panel gefärbten Objektträger auswertbar sind, kann
das Färbeergebnis von einem geschulten Pathologen unter
Heranziehung des Bewertungsalgorithmus ausgewertet werden.
HINWEIS: Als Nachweisreagenzien für die Verwendung mit dem
VENTANA MMR RxDx Panel werden nur OptiView DAB IHC
Detection Kit und OptiView Amplification Kit empfohlen.
10 VENTANA MMR RxDx Panel für Endometriumkarzinom

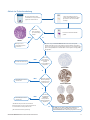
Ablauf der Probenbearbeitung
VENTANA MMR RxDx Panel für Endometriumkarzinom 11
4m dicke Schnitte werden auf
positiv geladene Objektträger gelegt.
(Es werden 6 oder 7 Serienschnitte
benötigt)
Färbung mit einer
neuen Patientenprobe
wiederholen*
Nein Ja
Ist die H&E-
Probe akzeptabel
(≥50lebensfähige
Zellen)?
Mit jedem Assay im VENTANA MMR RxDx Panel wird ein Schnitt gefärbt.
Zusätzlich wird für jeden Assay innerhalb desselben Gerätelaufs eine Färbung
mit einer speziesspezifischen negativen Reagenzkontrolle, einer Negative Control
(Monoclonal) (mNRC) bzw. einer Rabbit Monoclonal Negative Control Ig (rNRC)
durchgeführt.
Das MMR-Ergebnis (MLH1, PMS2, MSH2, MSH6) wird von
einem entsprechend geschulten Pathologen nach dem
VENTANA MMR RxDx Panel-Bewertungsalgorithmus bestimmt.
Nein
Nein
Nein
Ja
Ja
Ja
Ist der mit
der negativen
Reagenzkontrolle
gefärbte
Probenobjektträger
akzeptabel?
Weist jeder gefärbte
Probenobjektträger
akzeptable interne
Kontrollen auf?
Sind die mit
dem VENTANA
MMR RxDx
Panel gefärbten
Probenobjektträger
akzeptabel?
H&E-Färbung des
Tumors
Tumor-NRC
*Die Wiederholung kann mit demselben Block
Patientengewebe oder einem anderen Gewebeblock
desselben Patienten durchgeführt werden.
(Alle Tumorbilder in 20x Vergrößerung)
Interne Kontrolle
Tumor-IHC
Die Tumorgewebeprobe wird
6–72Stunden in 10%igem neutral
gepuffertem Formalin fixiert.
Ein Gewebeschnitt wird mit H&E
gefärbt.
Den Färbelauf wiederholen
Die Färbung dieses Falls
wiederholen*
Die Färbung dieses Falls
wiederholen*

12 VENTANA MMR RxDx Panel für Endometriumkarzinom
Referenzbilder
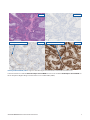
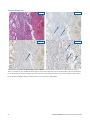
Fall1 mit positivem Expressionssignal: Status mit intakter Expression von MLH1, PMS2, MSH2 und MSH6 in einem
Endometriumkarzinom mit starker Zellkernfärbung in Tumorzellen bei akzeptablem Färbeergebnis interner Kontrollen. Bei den
dargestellten akzeptablen Negative Reagent Controls handelt es sich um Maus-NRC (mNRC) und Kaninchen-NRC (rNRC).
Fälle mit positivem
Expressionssignal
mNRC 20x
rNRC 20x
MLH1 20x PMS2 20x
MSH2 20x MSH6 20x
H&E 20x

VENTANA MMR RxDx Panel für Endometriumkarzinom 13
Fall2 mit positivem Expressionssignal: Status mit intakter Expression von MLH1, PMS2, MSH2 und MSH6 in einem
Endometriumkarzinom mit starker Zellkernfärbung in Tumorzellen bei akzeptablem Färbeergebnis interner Kontrollen. Bei den
akzeptablen Negative Reagent Controls handelt es sich um Maus-NRC (mNRC) und Kaninchen-NRC (rNRC).
H&E 20x
mNRC 20x rNRC 20x
MLH1 20x PMS2 20x
MSH2 20x MSH6 20x

14 VENTANA MMR RxDx Panel für Endometriumkarzinom
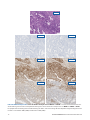
Fall1 mit defizienter Expression: Status mit Verlust der Expression von MLH1 und PMS2 in einem Endometriumkarzinom ohne
Zellkernfärbung in Tumorzellen bei akzeptablem Färbeergebnis interner Kontrollen. Die Expression von MSH2 und MSH6 ist intakt.
Die zytoplasmatische Färbung wird bei der Bestimmung des Status nicht berücksichtigt. Bei den akzeptablen Negative Reagent Controls
handelt es sich um Maus-NRC (mNRC) und Kaninchen-NRC (rNRC).
Fälle mit defizienter Expression
H&E 20x
mNRC 20x rNRC 20x
MLH1 20x PMS2 20x
MSH2 20x MSH6 20x

VENTANA MMR RxDx Panel für Endometriumkarzinom 15
Fall2 mit defizienter Expression: Status mit Verlust der Expression von MLH1 und PMS2 in einem Endometriumkarzinom ohne
Zellkernfärbung in Tumorzellen bei akzeptablem Färbeergebnis interner Kontrollen. Die Expression von MSH2 und MSH6 ist intakt.
Die zytoplasmatische Färbung wird bei der Bestimmung des Status nicht berücksichtigt. Bei den akzeptablen Negative Reagent Controls
handelt es sich um Maus-NRC (mNRC) und Kaninchen-NRC (rNRC).
H&E 20x
mNRC 20x rNRC 20x
MLH1 20x PMS2 20x
MSH2 20x MSH6 20x

16 VENTANA MMR RxDx Panel für Endometriumkarzinom
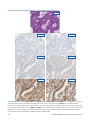
Fall3 mit defizienter Expression: Status mit Verlust der Expression von MSH2 und MSH6 in einem Endometriumkarzinom ohne
Zellkernfärbung in Tumorzellen bei akzeptablem Färbeergebnis interner Kontrollen. Die Expression von MLH1 und PMS2 ist intakt.
Die zytoplasmatische Färbung wird bei der Bestimmung des Status nicht berücksichtigt. Bei den akzeptablen Negative Reagent Controls
handelt es sich um Maus-NRC (mNRC) und Kaninchen-NRC (rNRC).
H&E 20x
mNRC 20x rNRC 20x
MLH1 20x PMS2 20x
MSH2 20x MSH6 20x
Seite wird geladen ...
Seite wird geladen ...
Seite wird geladen ...
Seite wird geladen ...
Seite wird geladen ...
Seite wird geladen ...
Seite wird geladen ...
Seite wird geladen ...
Seite wird geladen ...
Seite wird geladen ...
Seite wird geladen ...
Seite wird geladen ...
Seite wird geladen ...
Seite wird geladen ...
Seite wird geladen ...
Seite wird geladen ...
Seite wird geladen ...
Seite wird geladen ...
-
 1
1
-
 2
2
-
 3
3
-
 4
4
-
 5
5
-
 6
6
-
 7
7
-
 8
8
-
 9
9
-
 10
10
-
 11
11
-
 12
12
-
 13
13
-
 14
14
-
 15
15
-
 16
16
-
 17
17
-
 18
18
-
 19
19
-
 20
20
-
 21
21
-
 22
22
-
 23
23
-
 24
24
-
 25
25
-
 26
26
-
 27
27
-
 28
28
-
 29
29
-
 30
30
-
 31
31
-
 32
32
-
 33
33
-
 34
34
-
 35
35
-
 36
36
-
 37
37
-
 38
38
Roche BenchMark ULTRA Interpretation Guide
- Typ
- Interpretation Guide
- Dieses Handbuch eignet sich auch für
Verwandte Artikel
-
Roche VENTANA anti-ALK D5F3 Primary Antibody Benutzerhandbuch
-
Roche VENTANA PD-L1 (SP263) Assay, Universal, CE IVD, Predictive, NSCLC Interpretation Guide
-
Roche uPath PD-L1 image analysis for NSCLC IVD Algorithm Benutzerhandbuch
-
Roche uPath IVD Benutzerhandbuch
-
Roche NAVIFY Mutation Profiler Benutzerhandbuch







































